丂丂丂僈儔僗偲偼壗偐
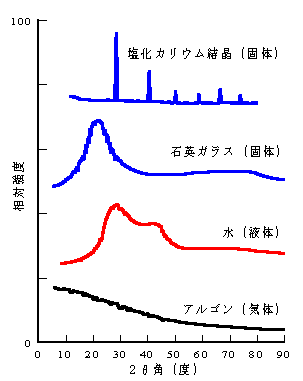
| 丂丂僈儔僗偲偼壗偐傪抦傞庤偑偐傝偲偟偰丄偼偠傔偵暔幙偺峔憿偵偮偄偰峫偊傑偡丅傛偔抦傜傟偰偄傞傛偆偵丄婎杮揑偵暔幙偼屌懱丄塼懱丄婥懱偺忬懺傪庢傝傑偡丅偦傟偧傟偺忬懺偱偺峔憿傪抦傞曽朄偼峔憿扨埵偺戝偒偝偲傎傏摨掱搙偺攇挿偺攇傪暔幙偵徠幩偟丄偦偺嶶棎偺條巕傪挷傋傞偙偲偱偡丅偦偺傕偭偲傕戙昞揑側曽朄偲偟偰倃慄夞愜偑偁偘傜傟傑偡丅壓偺恾偼扨尨巕婥懱偺傾儖僑儞丄塼懱偺悈丄屌懱偺愇塸僈儔僗偲墫壔僇儕僂儉寢徎偦傟偧傟偵偮偄偰丄CuK兛慄乮攇挿1.541侌乯傪巊偭偨倃慄夞愜偺寢壥偱偡丅墶幉偼俀兤丄廲幉偼夞愜嫮搙偱偡丅 |
| 丂丂 丂丂傾儖僑儞偱偼嫮搙偑妏搙偲偲傕偵扨挷偵尭彮偟偰偄傑偡丅偙傟偼奺尨巕偐傜嶶棎偝傟偨倃慄偺娫偱姳徛偑側偄偙偲傪帵偟偰偄傞偲峫偊傜傟傑偡丅偦偟偰姳徛偑側偄偲偄偆偙偲偼尨巕娫偵埵抲偺憡娭偑側偄偙偲丄尵偄姺偊傞偲丄偁傞弖娫偺尨巕偺埵抲傪幨恀偵嶣偭偨帪丄尨巕摨巑偼偍屳偄偵慡偔儔儞僟儉側埵抲娭學偵偁傞偙偲傪帵偟偰偄傑偡丅偦偟偰妏搙偲偲傕偵扨挷偵曄壔偡傞嶶棎嫮搙偼丄扨偵偁傞戝偒偝傪帩偮傂偲偮偺尨巕偐傜偺嶶棎偺條巕傪昞偟偰偍傝丄惓妋偵偼尨巕拞偱偺揹巕攝抲偵傛偭偰掕傑傞揹巕偺嬻娫揑側枾搙暘晍傪斀塮偟偰偄傑偡丅偙傟偼尨巕嶶棎場巕偲偟偰抦傜傟傞傕偺偵懳墳偟偰偄傑偡丅 丂丂墫壔僇儕僂儉寢徎偱偼丄偲傃偲傃偵塻偄僺乕僋偑尒傜傟傑偡丅偙傟偼峼暔寢徎偺櫆奐偐傜傕憐憸偝傟傞傛偆偵丄尨巕偑婯懃惓偟偔惍楍偟偰偄傞偨傔偵丄偁傞曽岦偱偼倃慄傪嬀偺傛偆偵斀幩偡傞尨巕柺偑偱偒傞偙偲偵傛傞偨傔偱偡丅偙偺偨傔摿掕偺曽岦偵嫮偄倃慄偺嶶棎偑婲偙傝傑偡丅偙傟傪Bragg嶶棎偲屇傃丄夞愜慄偼Bragg僺乕僋偲偟偰抦傜傟偰偄傑偡丅妏搙偑戝偒偔側傞傎偳斀幩偑庛偔側傞偺偼婥懱偺応崌偲摨條丄尨巕嶶棎場巕偺塭嬁偵傛傞傕偺偱偡丅 |
 |
| 丂丂 丂丂塼懱偱偁傞悈偺応崌偼丄婥懱偺傛偆偵扨挷偵偼曄壔偣偢嶶棎攇偺娫偵姳徛偑偍偒偰偄傞偙偲偑暘偐傝傑偡丅偟偐偟丄寢徎偺傛偆側Bragg僺乕僋偼懚嵼偟傑偣傫丅偙偺偙偲偼懡偔偺尨巕乮彮側偔偲傕1010屄掱搙乯偑偁傞婯懃惈偺壓偵惍楍偟偰偼偄側偄偑丄彮側偔偲傕壗傜偐偺拋彉偑懚嵼偡傞偙偲傪昞偟偰偄傑偡丅偦偟偰丄僺乕僋偺尰傟傞埵抲偐傜偙偺拋彉偑尨巕娫妘掱搙偱偁傞偙偲偑暘偐傝傑偡丅偡側傢偪丄塼懱偑棳摦惈傪帩偮偙偲偐傜傕悇應偝傟傞傛偆偵挿偄嫍棧偵傢偨偭偰婯懃惓偟偄尨巕攝抲傪曐偮乮挿嫍棧拋彉乯偙偲偼偱偒傑偣傫乮偙偺悢彮側偄椺奜偲偟偰塼徎偑偁偘傜傟傑偡乯丅堦曽丄塼懱偺枾搙偼屌懱偵嬤偔丄尨巕摨巑偼偍屳偄偵枾偵愙偟偰偄傑偡丅偙偺偨傔丄尨巕娫偵偼壔妛寢崌偑摥偒丄嵟嬤愙尨巕偺庬椶傗悢丄尨巕娫嫍棧偼寢徎偲偁傑傝戝偒偔偼曄傢傝傑偣傫乮壔妛揑抁嫍棧拋彉乯丅廬偭偰丄塼懱偱尒傜傟傞倃慄偺姳徛揑側嶶棎偼壔妛揑抁嫍棧拋彉傪斀塮偟偨傕偺偱丄偙傟傪夝愅偡傞偙偲偵傛傝嵟嬤愙尨巕娫嫍棧側偳偺忣曬偑摼傜傟傑偡丅 丂丂愇塸僈儔僗偼屌懱偱偡偑丄倃慄偐傜偼塼懱偲摨條偺峔憿傪帩偮傛偆偵尒偊傑偡丅掕惈揑偵偼偙偺傛偆側昤憸偼惓偟偄傕偺偱偁傝丄塼懱偑偦偺峔憿傪曐偭偨傑傑搥寢偝傟棳摦惈傪幐偭偨傕偺偑僈儔僗偱偁傞偲尵偊傑偡丅暔幙偺忬懺偲拋彉峔憿偺娭學傪傑偲傔傞偲懡偔偼埲壓偺傛偆偵側傝傑偡丅偙偙偱丄婥懱偼傾儖僑儞偺傛偆偵扨尨巕偱偐偮斾妑揑婓敄側忬懺傪峫偊偰偄傑偡丅傑偨丄挿嫍棧拋彉偲偼0.1乣1儈僋儘儞掱搙偵傢偨傞婯懃惈丄抁嫍棧拋彉偲偼嵟嬤愙偐傜戞俀嬤愙尨巕娫嫍棧掱搙丄拞嫍棧拋彉偼偦偺娫偺椞堟偱偡丅 |
| 忬懺 | 挿嫍棧拋彉 | 拞嫍棧拋彉 | 抁嫍棧拋彉 |
| 婥懱 | 亊 | 亊 | 亊 |
| 塼懱 | 亊 | 丠 | 仜 |
| 僈儔僗 | 亊 | 丠 | 仜 |
| 寢徎 | 仜 | 仜 | 仜 |
丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂偮偯偔
傕偭偲偔傢偟偔抦傝偨偄恖偺偨傔偺嶲峫彂乽僈儔僗傊偺桿偄丂旕徎懱偺壢妛擖栧乿丂撿搘挊丂丂嶻嬈恾彂丂(1993)乽僈儔僗壢妛偺婎慴偲墳梡乿丂嶌壴嵪晇挊丂丂撪揷榁掃曓丂(1997) |
尦偵栠傞